GUIÓN |
 |
Nuestro grupo de investigación se dedica a la búsqueda de nuevos agentes quimioterápicos, principalmente antitumorales y antiparasitarios. Ambas tienen en común que las células causantes de la enfermedad son eucariotas y se dividen sin respetar el control del hospedador.
Pese a los numerosos avances realizados en el tratamiento del cáncer en los últimos años éste continúa siendo la segunda causa de muerte. El cáncer es un conjunto heterogéneo de enfermedades, constituidas por células anormales que se dividen de forma descontrolada y se extienden a otros tejidos y órganos (metástasis). Por ello, nuestro objetivo es descubrir nuevos compuestos capaces de detener la proliferación incontrolada de los tumores, intentando no afectar a las células sanas.
Las enfermedades parasitarias afectan a miles de millones de personas y causan graves perjuicios para la salud. Nosotros nos dedicamos especialmente a las zoonosis, enfermedades que afectan a los seres humanos pero que también se extienden a los animales, que actúan como reservorios de la enfermedad. Muchas de estas enfermedades son enfermedades tropicales desatendidas (NTDs) para las que la OMS tiene planeada una estrategia global de control y erradicación, como la malaria, la leishmaniasis, la esquistosomiasis, la fasciolasis y otras... Todas estas enfermedades carecen de tratamientos o su tratamiento se basa en un único compuesto y además, están apareciendo resistencias que comprometen su eficacia terapéutica.
|
|
Con el fin de encontrar compuestos antitumorales y antiparasitarios, diseñamos compuestos capaces de impedir la proliferación celular indontrolada. Para ello hemos seleccionado una serie de proteínas esenciales para la proliferación de las células eucariotas, como la tubulina (la proteína que forma los microtúbulos y el huso acromático de la mitosis), la IMPDH (proteína que controla la síntesis de GTP), la NNMT (enzima que regula la concentración de nicotinamida) y las desacetilasas de lisinas (modificadoras postraduccionales -tras la síntesis de la proteína por el ribosoma- que regulan la expresión génica -epigenética- y la actividad de muchas otras proteínas).Por su gran importancia para el control de la división celular los tumores modifican el comportamiento de estas proteínas para promover su crecimiento, por lo que su inhibición puede conseguir actividad frente a los tumores. En los parásitos, las diferencias entre las proteínas del parásito y de los hospedadores facilitan el diseño de agentes selectivos.Además, trabajamos con análogos alquilfosfolípidos (APLs) que presentan una gran selectividad frente a células tumorales frente a células sanas. |
|
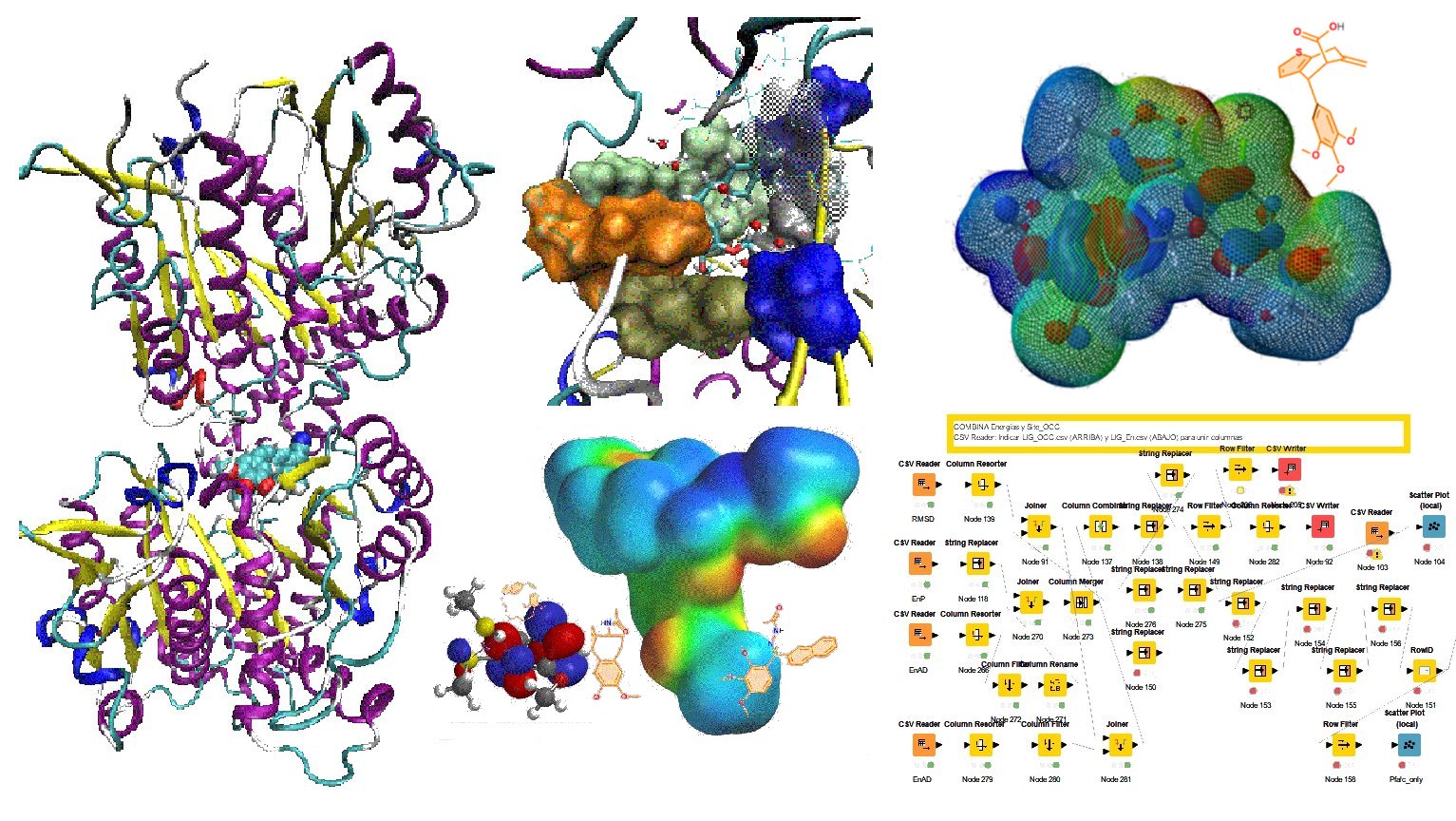
Diseñamos nuestros compuestos tomando como modelo productos naturales o ligandos conocidos (diseño basado en el ligando o LBDD) y los modificamos para incorporar nuevas actividades, mejorar su actividad y sus propiedades (solubilidad acuosa, estabilidad, etc) para que sw comporten como fármacos (drug-like). Para ello desarrollamos y utilizamos diversas técnicas de modelado molecular: relación estructura-actividad (REA) para cada tipo de diana, modelos de interacción, variación controlada de propiedades...Utilizando la estructura 3D de las dianas hacemos diseño basado en la estructura (SBDD). Para tubulina, IMPDH y NNMT tenemos colaboradores que determinan la estructura de las dianas y de los complejos con nuestros ligandos. Empleamos metodologías de docking y dinámica molecular para ver cómo interaccionan los compuestos antes de sintetizarlos con sus dianas.Diseñamos compuestos que presentan más de un mecanismo de acción (fármacos de acción múltiple). Para ello, combinamos los requerimientos para ejercer cada actividad en una misma molécula.También proporcionamos a nuestros compuestos la capacidad de incorporarse a nanopartículas (NPs).Además, incorporamos fluorescencia en el diseño de los compuestos para poder seguirlos en los ensayos biológicos y estudiar su mecanismo de acción. |
 |
Sintetizamos los compuestos seleccionados utilizando rutas sintéticas que nos permitan obtener series de compuestos con modificaciones en distintos puntos de la estructura, para poder explorar la relación estructura actividad (REA) de las nuevas familias de compuestos (puedes encontrar ejemplos concretos en nuestros TFMs, TFGs, trabajos de iniciación a la investigación, etc.... o en nuestras publicaciones). Entre los tipos de compuestos que sintetizamos se encuentran las sulfonamidas, las amidas, compuestos heterocíclicos, análogos de fosfolípidos, análogos de lisinas acetiladas, análogos de nucleótidos y dinucleótidos y otros. Además, modificamos los componentes para explorar la REA, introduciendo diversos sustituyentes y funcionalidades. Para ello utilizamos síntesis robustas que nos permiten variar la estructura de los reactivos. |
Un ejemplo de síntesis son las benzofenonas. Por su actividad antitumoral reciben el nombre de fenstatinas (fen- de benzofenona y -statin de inhibidor de la proliferación). Se obtienen mediante una reacción de Grignard entre un derivado organometálico y un aldehído. Se obtienen así diarilalcoholes que se oxidan para dar las cetonas. A partir de las cetonas hacemos numerosas modifiaciones que conducen a compuestos muy activos. Además introducimos diversas modificaciones en los anillos (hetero)aromáticos Ar1 y Ar2. |
 |
En nuestro laboratorio realizamos diversos ensayos biológicos para evaluar los nuevos compuestos sintetizados. Evaluación como antitumorales: Realizamos ensayos frente a distintas líneas celulares tumorales humanas (de cólon, mama, útero, glioblastomas, hepáticos,...) y determinamos la concentración de compuesto que inhibe el 50% de la proliferación de cada línea celular. Además estudiamos si los compuestos son expulsados de las células tumorales por proteínas de resistencia múltiple (MDR), para seleccionar sólo aquellas familias que no los son. Para los compuestos activos estudiamos los mecanismos de acción. Estudiamos cómo ejercen su acción sobre las células tumorales mediante inmunofluorescencia y citometría de flujo. Además estudiamos el efecto sobre las dianas (en la figura se muestra un ensayo frente a la tubulina). |
|
Evaluación como antiparasitarios: Realizamos ensayos frente leishmaniasíneas celulares tumorales humanas en distintos estadíos (promastigotes de vida libre y amastigotes intracelulares). También realizamos ensayos frente a Strongyloides venezuelensis en colaboración con el departamento de Parasitología. Determinamos la concentración de compuesto que matan el 50% de los parásitos. Además estudiamos si los compuestos son captados o no por los parásitos multicelulares (helmintos) y la localización de los compuestos en los parásitos mediante microscopía de fluorescencia. Para los compuestos activos estudiamos los mecanismos de acción. Estudiamos cómo ejercen su acción sobre las células tumorales mediante inmunofluorescencia y citometría de flujo. Además estudiamos el efecto sobre las dianas (en la figura se muestra un ensayo frente a la tubulina). |
 |
Evaluación de propiedades farmacocinéticas: Realizamos ensayos para determinar si los compuestos sintetizados presentan propiedades tipo fármaco (drug-like). Esto nos permite descartar aquellos tipos de compuestos que no presenten propiedades adecuadas para su administración: solubilidad en agua y distintos tampones, estabilidad química en agua y distintos tampones y frente al metabolismo hepático y absorción. Esto reduce las posibilidades de fracaso en los ensayos in vivo. También estudiamos el comportamiento de las nanopartículas y la inclusión de nuestros compuestos en ellas. |